【アクテムラとわが研究人生 vol.31 驚異的な有効率】
2025.04.01
驚異的な有効率
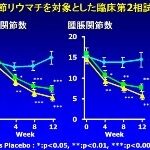
日本で実施された関節リウマチを対象とした臨床第II相試験の成績。プラぜボ(♦印)、MRA4mg/kg(■印)、およびMRA8mg/kg(▲印)を
0、4、8週の計3回、静脈内に点滴注射した。
左図に疼痛関節数、右図に腫脹関節数の推移を示すが、試験開始後12週目まで投与するたびに症状は改善し、
8mg/kgの方が4mg/kgよりも高い効果を示した(Nishimoto et.al.,Arthritis and Rheum.50:1761-69,2004)
1995年、大きな組織改正が実施され5つの創薬研究所が1つにまとめられた。私は、7年半の単身赴任生活を終えると同時に、入社後初めて研究所組織の外側に出ることになった。新しい所属は本社の研開企画部である。東京都小平市中島町の自宅から本社まで、最寄り駅の西武拝島線東大和駅で乗車し、高田馬場駅で地下鉄東西線に、日本橋で地下鉄銀座線に乗り換えて京橋駅に出た。1時間15分も満員電車に揺られ通勤するのもそうだったが、それよりも何よりも、だだっ広いオープンスペースにたくさんの机が並んだオフィスで前に座る人と向かい合わせで仕事をするのは、大きなカルチャーショックだった。周りでの話し声が耳に入るし、他人の目が気になって科学論文や資料などを集中して読むのが難しかった。それでも毎日のように午後になると自席ですやすやとお眠りする豪傑がちらほら見受けられたが、すごい人だと変に感心したりもした。
余談だが、本社勤務が始まって間もない時期に、ヘッドハンターから連絡があった。それまでにも何度か転職の誘いを受けたことがあったが、具体的な会社名や職務内容など聞くこともなく「興味がありません」とお断りしていた。しかし、今回の誘いは違っていた。会社名を告げた上に、新しく開設する研究所の所長になってほしいという極めて具体的な話であった。「長年続けた研究生活から本社勤務になったことにさぞかし寂しさを感じ不満を持っているのではないか」と私の心中を想像しての勧誘だったのかもしれないが、私には大切なMRA(後のアクテムラ)があり、MRAの成功を見届けるまでは会社を離れられなかった。電話でのお話だったのでその場で丁重にお断りした。
さて、待ちに待ったマスターセルバンク(MCB)用の細胞株は、96年になって無事に樹立されたとの報告が研究所から本社に届いた。牛海綿状脳症(BSE)問題が契機となった無血清培養法技術の確立や大量培養での生産量を高める技術の検討などは大変な難業であったが、生産技術関係者の総力を挙げての努力で満足できるレベルに達した。
レミケードの日本進出に伴い多発性骨髄腫の治療薬として開発が進められてきたMRAの開発方針が、関節リウマチ治療薬としての応用へと大きくかじを切ったのは前回で述べた通りである。96年 に、研究本部内での探索研究提案「MRAの関節リウマチ適用について」、創薬研究所と研開企画部が合同で提出した研究提案書「MRAの慢性関節リウマチ適用に関する研究」、そしてRDM会議において研開企画部から付議された開発提案「MRA(慢性関節リウマチ)国内・海外」が、矢継ぎ早に承認された。第29回で述べたマウスやサルにおけるコラーゲン関節炎に対する抑制効果が明らかになったことも、RDM会議での決議を後押しした。
臨床試験を実施するために必要な有効性、安全性、薬物動態などの非臨床試験を終え、健常人での臨床第I相試験が97年に開始された。その結果、問題となるような副作用が認められなかったので、次に関節リウマチ患者を対象に臨床第I/II相試験が実施された。この試験で得られたファーマコキネティクス(薬力学)のデータに基づき薬物投与量が設定され、2001年に関節リウマチ患者を対象とした第II相試験に移行した。大阪大学の吉崎和幸先生が治験調整医師、西本憲弘先生が医学専門家を務めた。02年5月、別室でキーオープンの作業が完了し、有効性を示すグラフが世話人会の待つ部屋の大きなスクリーンに映し出されると、出席していた中外製薬社員からどよめきが起こった。MRAを投与された患者の78 %が症状改善を示すという驚くべき高い有効率を示す棒グラフが目に飛び込んできたからだ(Nishimoto et.al.,Arthritis and Rheum.50:1761-69,2004)。「90%を超えると思ったんやけどなー」と残念そうに言った西本先生の言葉が今も印象に残っている。
この成績は02年の米国リウマチ学会(ACR)年次集会で急きょ発表されるが、一部の専門家を除き実はさほどの関心を集めたわけではなかった。当時の学会ではエンブレルやレミケードなどのTNFα阻害薬の有効性が大きな注目を集め、関節リウマチの発症・病態の進展にTNFαが大事な役割を演じることに、学会のコンセンサスが得られていた。
この年次集会で、著名なリウマチ専門家の特別講演を拝聴した時に、スライドを見てびっくりしたのを思い出す。そのスライドは、リウマチの症状がサイトカイン類のバランスの崩れによって悪化するということを説明するために作成されたものであった。サイトカインは向炎症性サイトカインと抗炎症性サイトカインに分けられ、前者に属するものとしてTNFαやIL1が、後者にはIL1ra(receptor antagonist)と呼ばれる生体内に存在する自然のIL1阻害因子やIL10などが記載されており、なんとIL6は抗炎症性サイトカインの部類に入れられていた。すなわち、関節滑膜に多量に検出されたIL6は、そこでの炎症を抑え終息させるために産生されると理解されていたのである。それから1年から2年後の同じ学会では先の講演者とは異なる演者が、IL6をシーソー台の中央(支点)の真上に記載した図を示した。向炎症性とも抗炎症性とも決めかねていたのである。
そういう状況だったので、欧米の大手製薬企業もMRAの劇的な効果をにわかには信じ難く、興味を示さなかったのだろう。MRAが欧米で評価を受けるようになったのは欧州での第II相試験で高い有効性が確認されて以降のことである。
そんな中でMRAに触手を伸ばしたのがスイスRoche社だった。国内第II相試験が終了し、ヨーロッパでの第II相試験が続行中の02年に、中外はRoche社の傘下に入った。Roche社が中外株式の50.1%を保有し、中外は日本ロシュと統合 し、中外製薬という社名を残して経営の自立性を与えられた。新しいタイプの企業間合併として世の注目を集めた。これにより、Roche社が中外のプロジェクトの全てに対して第一拒否権(First refusal right)を獲得した。
Roche社はMRAに興味を示した。臨床開発担当のリウマチ専門医学博士が来日し、臨床試験のデータ・数値を症例1例ごとに細かくレビューした。レビューは何日もの時間をかけて徹底的に行われた。博士は、関節リウマチ患者を対象にした抗CD20抗体「リツキシマブ」の臨床試験を担当した経験があり、MRAの評価には最適の人物だったと思う。彼とRoche社は、B細胞を抑制するという点で、リツキシマブとMRAとが共通の作用機序を有する点に興味を抱いたのであろうと、私は思っている。
この時、Roche社側が懸念した材料としては、大きくは2つあった。1つは欧米で実施されている臨床第II相試験で、日本で得られた結果を裏付けるような良好な成績が得られるのかどうかであった。日本とはリウマチの治療体系に違いがあり、患者背景も異なるからである。他の1つは特許残存期間が短いことであった。莫大な開発費用をかけて開発するのであるから、特許期間は長ければ長いほど良い。 しかし、抗体医薬のようなバイオ医薬品のジェネリック、いわゆるバイオシミラーの開発は容易ではない。この読みがRoche社の決断を促したのかもしれない。
03年、Roche社は中外が欧州で実施した第II相試験(Charisma試験)の結果から、MRAの難治性関節リウマチに対する有効性を確信したようである。MRAの欧米、並びに中国での開発を決定し、中外とのMRA共同開発契約が締結された。
初出:日経バイオテクONLINE 2017年4月17日掲載。日経BPの了承を得て掲載










