【アクテムラとわが研究人生 vol.7 逃した大魚】
2024.10.15
逃した大魚
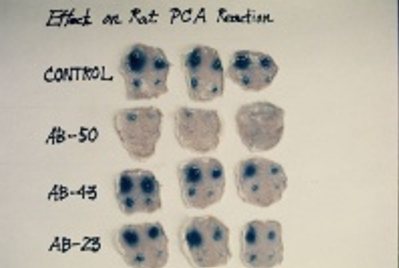
ラット背部皮膚を剥ぎ取って内面の青色斑(アレルギー反応により血管透過性が亢進すると
血管から青色色素が血管外に漏出する)を撮影したもの。個体ごとに4つの斑点があるが、
上左から上右、下左、下右とIgE抗体量が2倍階段希釈されている。
AB50が経口投与で強い抑制作用を示している。AB-23は経口投与では無効である
ラット背部皮膚を剥ぎ取って内面の青色斑(アレルギー反応により血管透過性が亢進する
と血管から青色色素が血管外に漏出する)を撮影したもの。個体ごとに4つの斑点があるが、
上左から上右、下左、下右とIgE抗体量が2倍階段希釈されている。
AB50が経口投与で強い抑制作用を示している。AB-23は経口投与では無効である

マウス個体ごとに摘出された腫瘍塊。OK-432(ピシバニール)の抗腫瘍効果は、
抗リンパ球血清(ALS)注射により減弱している
前回記した内容と重複するが、ミコフェノール酸の免疫抑制作用に関して、マウスへの皮膚移植実験の際にその投与時期を変えて効果発現との関係を調べ、免疫が既に成立した時期から投与を始めても拒絶反応が抑制されることを見いだした。つまり、ミコフェノール酸は免疫の誘導を抑制する作用の他に、既に成立した免疫反応によって誘起される炎症、あるいはアレルギー反応を抑制することが示唆されたのである。移植前から薬物を投与した場合には、免疫反応の阻害に伴い拒絶反応が抑制されるのは当然だが、免疫が成立した後に投与を始めても拒絶反応が抑制されるというのは予想外の結果だった。
この発見は、米国シリコンバレーに在ったSyntex社(現在はスイスRoche社グループの一員)の研究者の興味を引いたのではないかと私は推測しているが、成果を報告したのは「移植」誌と「アレルギー」誌という日本語の学術誌のみだったので果たして彼らの目に留まったかどうか定かではない。いずれにせよ彼らは後に、ミコフェノール酸モフェチル(ミコフェノール酸の誘導体)の医薬品としての開発に成功している(日本では中外製薬が「セルセプト」として発売)。当時、臓器移植に伴う免疫拒絶反応は「プログラフ」(タクロリムス)を術前から投与することでかなりコントロールできるようになっていたが、ミコフェノール酸モフェチルは拒絶反応が起こってから投与しても効果が得られるという既存薬に無い利点を持っていた。このユニークな効果が評価され、セルセプトはブロックバスターに成長した。
私は、ミコフェノール酸誘導体が重篤な下痢という副作用を有することに気が付いて開発の継続を諦めた。しかし、Syntex社は、この化合物のユニークな作用に着目して開発を諦めなかったのだろう。私の粘り強さが不足していたというよりも、当時、日本で臓器移植がそれほど行われていなかったことが、私の執着心を弱めたのだと思う。
私はミコフェノール酸誘導体を臓器移植片に対する拒絶反応阻害薬として開発することを断念したが、一方で抗アレルギー作用に着目して作用機序に関する研究を進めた。その結果、ミコフェノール酸の作用は、免疫溶血反応阻害作用(抗補体作用)、細胞膜安定化作用、血小板凝集阻害作用、遅延型反応阻害作用など多岐にわたることが判明した。ミコフェノール酸誘導体は前述した馬杉腎炎モデルの動物にも有効性を発揮した。
中でも注目されたのは、赤血球の免疫溶血反応阻害作用である。
そこで、前出の森さん、高久さんという2人の合成研究員と共に数多くのミコフェノール酸誘導体を合成し、それらの免疫溶血反応阻害活性をテストし、その中から、より活性の高い化合物を選び、構造活性相関を検討した上で、さらに誘導体を合成するという作業を繰り返し、繰り返し行った。私は素人なりに、化合物の構造に口を挟むと、「大杉さんは、生物屋なのに化学構造式が読める」と感心された。置換基の種類や置換位置など自由な発想に基づき提案すると、よく彼らは、「それは合成が極めて難しいね」と言って、その日の検討会は終了するのであるが、数日後には必ず「合成に成功した!」との連絡が来た。優秀な合成化学者と巡り合えて幸せであった。
このようにして極めて低濃度で強い作用を有する化合物AB-23を見つけた。また、興味深いことにAB-23は、ヒツジの赤血球を60℃で20分間加熱することによって引き起こされる溶血反応に対しても阻害作用を有していた。
当時、私の直属の上司だった免疫研究室長の松野隆さんと一緒に、岩手医科大学の光井庄太郎教授を訪れ相談したところ、抗アレルギー薬としての可能性があるのではというアドバイスを受けた。藤沢薬品工業(現アステラス製薬)が英Fison社から導入した「インタール」(クロモグリク酸)という気管支喘息治療薬が肥満細胞の膜安定化作用を介してヒスタミンの細胞外遊離を抑制することが知られていたからである。
光井先生からは日本医科大学の木村義民教授を紹介され、抗アレルギー作用の評価方法を習った。IgE抗体で感作された肥満細胞からのヒスタミン遊離を調べるPCA(Passive Cutaneous Anaphylaxis)反応という皮内反応で、抗原としてブタ回虫成分を用いた。AB-23は見事にこの反応を阻害した。しかし、残念ながら経口投与では効果が認められなかったので、消化管からの吸収を高める必要が生じた。そのための誘導体が合成され、最終的にAB-50という開発コード名を付けられた化合物の創製に行き着いた。
AB-50(その生体内活性体であるAB-23)は、抗補体作用や肥満細胞膜安定化によるI型アレルギー抑制作用、実験的腎炎抑制作用(II型アレルギー抑制作用)など多彩な作用を有していた。中でも特に、III型アレルギーであるアルサス反応やⅣ型の遅延型アレルギーを阻害することに周囲の関心は集まった。1976年9月22日から盛岡市で開催された日本アレルギー学総会のワークショップ「抗アレルギー剤の基礎と臨床」で我々が発表した際に、司会をされた岐阜薬科大学の江田昭英教授から、「AB-50の広範囲な作用が競合品と比較して臨床でどのような差が出るのか注目される」、とのコメントを頂いた。江田教授らが中心となって開発していた「リザベン」(トラニラスト、その後82年にキッセイ薬品工業が販売開始)や、東洋醸造(現旭化成)、武田薬品工業が開発中のものは、いずれもインタールと同様の肥満細胞の膜安定化作用を有するI型アレルギー阻害薬だったからだ。だがAB-50は、光井先生を中心に数施設で実施された喘息患者での初期第II相試験において臨床効果を示唆する成績が得られたが、残念ながら肝毒性のために開発が中止となった(79年)。
会社は諦めきれずに、AB-50の副作用を軽減した改良品の合成を継続した。AM-682と名付けられた化合物はI型(即時型)アレルギー反応に対してはAB-50をしのぐ阻害作用を有していたが、アルサス反応や遅延型反応を抑制する効果は無かった。87年に実施された多施設二重盲検比較臨床第III相試験において比較対照群との間に統計学的に有意な有用性が認められずに開発中止となった。中止に追い込まれたのは残念だったが、非臨床試験から臨床第III相試験に至る一連の過程を一通り体験できたことが大きな自信・財産となり将来の研究に役立った。
溶連菌製剤「ピシバニール」の本質
少し話は戻るが、入社翌年に当たる70年に綜合研究所研究部内に「免疫研究室」が新設された。免疫学研究領域は将来の発展が見込まれ、製薬企業でも免疫反応を調節する薬剤の探索研究が重要な位置を占めるであろうと考えたのだろう。日本免疫学会が発足する前年のことであり、当時の研究所幹部の先見の明に感服せざるを得ない。メンバーは私を入れて3人だった。1人は血液凝固線溶系を専門とする研究者で、もう1人が室長の松野さんだった。松野さんの専門領域は微生物学で、溶連菌製剤「ピシバニール」の研究に従事し、米国シカゴ郊外にあるNorthwestern Universityに留学中であった。71年に帰国後、AB-50の研究に始まり、アクテムラの研究開発を含めて長い期間にわたって私の直属の上司となった。
ピシバニールは宿主介在性抗腫瘍薬という新しいコンセプトを標榜するユニークな薬剤である。宿主介在性を証明する実験系を考案することが私の課題で、やがてリンパ球の欠損状態ではピシバニールは抗腫瘍効果を十分に発揮できないのではないかとの考えが浮かんだ。そこで、マウスのリンパ球をウサギに注射して抗体を作製し、この抗体をマウスに注射するとリンパ球が減少することが判ったので、その条件でピシバニールが抗腫瘍効果を発揮するか否か検討した。すると予想通り、効果は減弱した。ピシバニールは宿主のリンパ球が正常状態に存在しなければ、十分な効果を発揮できないことが証明されたのである。抗リンパ球抗体の作製には、かつて馬杉腎炎惹起抗体で苦労した経験が生かされたのは言うまでもない。
初出:日経バイオテクONLINE 2016年10月24日掲載。日経BPの了承を得て掲載










